Electrolyzer
Ang electrolysis ay isang kemikal-pisikal na kababalaghan ng agnas ng mga sangkap sa mga elemento na gumagamit ng isang kasalukuyang kuryente, na ginagamit saanman para sa mga hangaring pang-industriya. Batay sa reaksyong ito, ang mga pinagsama ay ginawa upang makakuha, halimbawa, klorin o mga di-ferrous na metal.

Halaman ng electrolysis, na binubuo ng mga plato
Ang patuloy na paglaki ng mga presyo para sa mga mapagkukunan ng enerhiya ay gumawa ng mga ionic na pag-install para sa pangangailangan sa bahay. Ano ang mga naturang istraktura, at kung paano ito gawin sa bahay?
Pangkalahatang impormasyon tungkol sa electrolyser
Ang isang planta ng electrolysis ay isang aparato para sa electrolysis na nangangailangan ng isang panlabas na mapagkukunan ng enerhiya, na istrakturang binubuo ng maraming mga electrode, na inilalagay sa isang lalagyan na puno ng electrolyte. Gayundin, ang pag-install na ito ay maaaring tawaging isang aparato ng paghahati ng tubig.
Sa mga katulad na yunit, ang pagiging produktibo ay itinuturing na isang pangunahing panteknikal na parameter, na nangangahulugang ang dami ng hydrogen na ginawa bawat oras at sinusukat sa m3 / h. Ang mga nakatigil na yunit ay nagdadala ng gayong parameter sa pangalan ng modelo, halimbawa, ang SEU-40 membrane unit ay bumubuo ng 40 cubic meter bawat oras. m ng hydrogen.


panlabas na pagtingin ng nakatigil na pang-industriya na yunit ng SEU-40
Ang iba pang mga katangian ng naturang mga aparato ay ganap na nakasalalay sa inilaan na layunin at ang uri ng pag-install. Halimbawa, kapag gumaganap ng electrolysis ng tubig, ang kahusayan ng yunit ay nakasalalay sa mga sumusunod na tagapagpahiwatig:
- Ang antas ng pinakamababang potensyal na elektrod (boltahe). Para sa isang mahusay na paggana ng yunit, ang katangiang ito ay dapat nasa saklaw na 1.8-2 V bawat plato. Kung ang suplay ng kuryente ay may boltahe na 14 V, kung gayon ang kapasidad ng electrolytic cell na may electrolyte solution ay may katuturan upang hatiin ang mga sheet sa 7 mga cell. Ang isang katulad na pag-install ay tinatawag na isang dry cell. Ang isang mas maliit na halaga ay hindi magsisimula sa electrolysis, at ang isang mas malaking halaga ay lubos na madaragdagan ang pagkonsumo ng enerhiya;
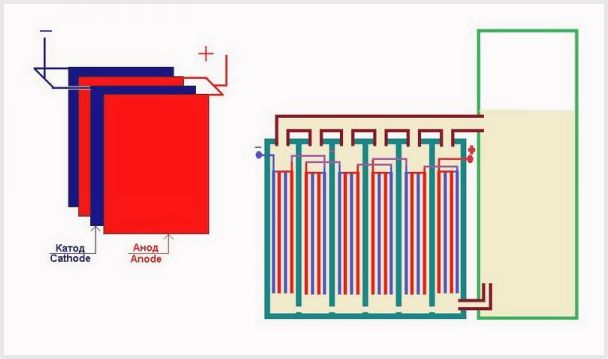

Pag-aayos ng mga plato sa paliguan ng isang planta ng electrolysis
- Ang mas maliit na distansya sa pagitan ng mga elemento ng plate, mas mababa ang paglaban, kung saan, kapag ang isang malaking kasalukuyang pumasa, ay humahantong sa isang pagtaas sa paggawa ng gaseous na bagay;
- Ang ibabaw na lugar ng mga plato ay direktang nakakaapekto sa pagiging produktibo;
- Ang balanse ng init at antas ng konsentrasyon ng electrolyte;
- Materyal ng mga bahagi ng elektrod. Ang ginto ay itinuturing na isang mamahaling ngunit kahanga-hangang materyal para magamit sa mga electrolytic cell. Dahil sa mataas na gastos, minsan ay ginagamit ang hindi kinakalawang na asero.
Ang pangunahing bagay! Sa mga konstruksyon ng iba't ibang uri, ang mga halaga ay magkakaroon ng magkakaibang mga parameter.
Ang mga halaman ng electrolysis ng tubig ay maaari ding gamitin para sa mga layunin tulad ng pag-decontamination, paglilinis at pagtatasa sa kalidad ng tubig.
Pagkuha ng hydrogen sa laboratoryo
Ang modernong pamamaraan ng laboratoryo para sa paggawa ng hydrogen ay hindi naiiba mula sa kung saan ito nakuha ng Henry Cavendish. Ito ang mga reaksyon ng mga metal na may mga asido. Sa laboratoryo, ang hydrogen ay nakuha sa patakaran ng pamahalaan Kippa (Larawan 152).
Aparatong Kipp gawa sa salamin at binubuo ng maraming bahagi:
- reaksyon ng prasko na may reservoir;
- funnel na may isang mahabang tubo;
- tubo ng gas outlet.
Ang flask ng reaksyon ay may isang itaas na spherical na bahagi na may isang pambungad kung saan ang isang gas outlet tube na nilagyan ng tap o clamp ay ipinasok, at isang mas mababang reservoir sa anyo ng isang hemisphere. Ang mas mababang reservoir at ang reaksyang prasko ay pinaghihiwalay ng isang goma o plastik na gasket na may isang butas kung saan ang isang mahabang tubo ng funnel ay umaabot sa mas mababang reservoir, na umaabot hanggang sa ilalim. Ang mga solido (marmol, sink) ay ibinuhos papunta sa gasket sa pamamagitan ng butas sa gilid na may isang spatula.Ang butas ay sarado na may isang plug na may isang gas outlet tube. Pagkatapos, sa pagbukas ng tap o clamp, ang acid solution ay ibinuhos sa itaas na funnel. Kapag naabot ng antas ng likido ang sangkap sa gasket, nagsisimula ang isang reaksyong kemikal sa paglabas ng gas. Kapag nakasara ang balbula, pinipilit ng presyon ng nagbago na gas ang likido palabas ng reaktor papunta sa tuktok ng funnel. Humihinto ang reaksyon. Ang pagbukas ng gripo ay humahantong sa pagpapatuloy ng reaksyon. Ilagay ang mga piraso ng sink sa reaksyang prasko. Gagamitin namin ang sulfuric acid bilang acid. Sa pakikipag-ugnay ng sink at sulfuric acid, nangyayari ang sumusunod na reaksyon:
Zn + H2SO4 = ZnSO4 + H2
Maaari mong punan ang isang bubble ng sabon ng hydrogen.
Upang magawa ito, kinakailangang ibaba ang flue gas pipe sa isang solusyon na may sabon. Sa pagtatapos ng tubo, isang bubble na sabon na puno ng hydrogen ay magsisimulang mabuo; sa paglipas ng panahon, ang bubble ay nasisira at lumilipad paitaas, na nagpapatunay sa gaan ng hydrogen. Kolektahin natin ang nagbabagong hydrogen... Isinasaalang-alang na ang hydrogen ay mas magaan kaysa sa hangin, upang makolekta ang hydrogen, ang sisidlan kung saan kinokolekta ang gas ay dapat ilagay sa baligtad, o dapat itong kolektahin ng pag-aalis ng tubig. Paano makahanap ng hydrogen? Punan ang tubo ng hydrogen, hawakan itong baligtad na may kaugnayan sa tubo ng gas outlet. Dinadala namin ang test tube na may isang butas sa apoy ng lampara ng espiritu - naririnig ang isang katangian na pop.
Bulak - Ito ay isang palatandaan na ang test tube ay naglalaman ng hydrogen. Kapag ang test tube ay dinala sa isang apoy, ang hydrogen ay tumutugon sa oxygen sa hangin. Sa maliit na halaga, ang reaksyon ng oxygen at hydrogen ay sinamahan ng isang pop. Higit pang mga detalye tungkol sa reaksyong ito ay tatalakayin sa susunod na talata.
Nagtatrabaho prinsipyo at mga uri ng electrolyzer
Ang isang napaka-simpleng aparato ay may mga electrolyzer na nahahati sa tubig sa oxygen at hydrogen. Binubuo ang mga ito ng isang lalagyan na may isang electrolyte kung saan inilalagay ang mga electrode, na konektado sa isang mapagkukunan ng enerhiya.
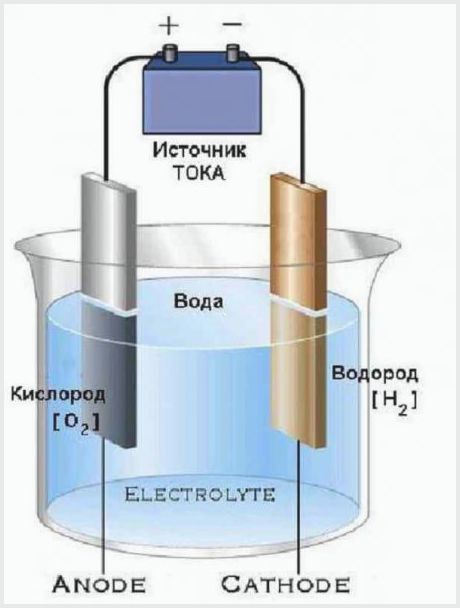

Ang disenyo ng pinakasimpleng planta ng electrolysis
Ang prinsipyo ng pagtatrabaho ng isang halaman ng electrolysis ay ang kasalukuyang kuryente na dumadaan sa electrolyte ay may boltahe na sapat upang mabulok ang tubig sa mga molekula. Ang resulta ng proseso ay naglalabas ang anode ng isang bahagi ng oxygen, at ang cathode ay lumilikha ng dalawang bahagi ng hydrogen.
Ang electrolysis ng tubig sa mga industrial hydrogen generator
Elektrolisis
ito ay isang reaksyon ng redox na nagaganap lamang sa ilalim ng impluwensya ng kuryente. Sa mga industrial hydrogen generator, ang electrolysis ng tubig ay isinasagawa upang makakuha ng hydrogen at oxygen. Upang magpatuloy ang reaksyon, dapat ilagay ang dalawang electrodes sa electrolyte, na konektado sa isang mapagkukunan ng kuryente ng DC:
- Anode
- elektrod kung saan nakakonekta ang positibong konduktor; - Cathode
- ang elektrod kung saan nakakonekta ang negatibong conductor.
Nasa ibaba ang isang eskematiko diagram ng isang pang-industriya na alkaline electrolyser.
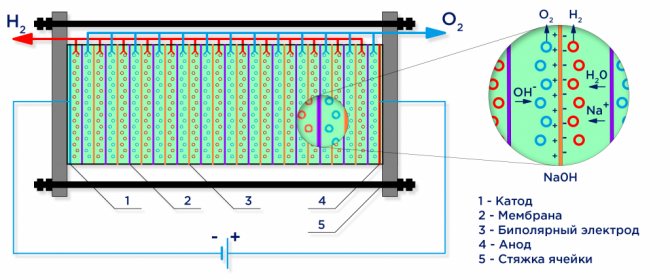

Electrolysis ng tubig
Sa ilalim ng pagkilos ng isang kasalukuyang kuryente, ang tubig ay nahahati sa mga sangkap na bumubuo nito: hydrogen at oxygen. Ang isang negatibong sisingilin na katod ay nakakaakit ng mga hydration cation, at ang isang positibong sisingilin na anode ay nakakaakit ng mga OHion.
Ang demineralisadong tubig na ginamit sa mga pang-industriya na halaman ng electrolysis ay isang mahina na electrolyte, kaya idinagdag dito ang mga malalakas na electrolyte upang madagdagan ang kondaktibiti ng kasalukuyang kuryente. Kadalasan, ang mga electrolyte na may mas mababang potensyal na cationic ay pinili upang maibukod ang kumpetisyon sa mga hydrogen cation: KOH o NaOH. Ang electrochemical reaksyon na nagaganap sa mga electrode ay ang mga sumusunod:
- Reaksyon ng anode: 2H2O → O2
+ 4H + + 4e− - oxygen evolution; - Reaksyon ng Cathode: 2H2O + 2e− → H2
+ 2OH− - evolution ng hydrogen.
Ang isang pang-industriya na electrolyzer ay binuo ayon sa isang bipolar scheme, kung saan ang mga bipolar "intermediate" electrode na may iba't ibang mga singil sa mga gilid ay inilalagay sa pagitan ng pangunahing electrode at cathode.Sa gilid ng pangunahing anode, ang intermediate electrode ay may gilid na katod, sa gilid ng katod - isang gilid ng anode (tingnan ang pigura).
Dagdag dito, upang makakuha ng purong hydrogen at oxygen, kinakailangan upang paghiwalayin ang mga gas na nabuo sa mga electrode, at para dito, ginagamit ang paghihiwalay na mga membranes ng exchange ng ion (tingnan ang pigura). Ang dami ng hydrogen na nagawa ay dalawang beses ang dami ng oxygen na nagawa, at samakatuwid ang presyon sa lukab ng hydrogen ay tumataas nang dalawang beses nang mas mabilis. Upang mapantay ang presyon sa mga lukab, ang isang presyon na pantay na lamad ay ginagamit sa labasan ng electrolyzer, na pumipigil sa pagpuga ng hydrogen sa lukab ng oxygen sa pamamagitan ng mga channel na inilaan para sa sirkulasyon ng electrolyte.
Ang pamamaraang ito ay ang pinakalawakang ginagamit na pamamaraan sa industriya at ginagawang posible upang makakuha ng gas na hydrogen na may kahusayan ng 50 hanggang 70% na may kapasidad na hanggang 500 m3 / h sa isang tiyak na pagkonsumo ng enerhiya na 4.5-5.5 N2m3 / kWh.
Elektrikal sa TPE
Sa kasalukuyan, ang pinakamabisang pamamaraan ng paghihiwalay ay ang electrolysis na gumagamit ng solidong polymer electrolytes batay sa isang perfluorinated ion exchange membrane.
Pinapayagan ng ganitong uri ng electrolyser ang produksyon ng hydrogen na may isang kahusayan ng hanggang sa 90% at ang pinaka-environment friendly. Ang mga electrolyzer na may TPE ay 6-7 beses na mas mahal kaysa sa mga alkalina, at samakatuwid ay hindi pa nagkakalat sa industriya.
Mga uri ng electrolyzer
Ang mga aparato para sa paghahati ng tubig ay sa mga sumusunod na uri:
Ang mga electrolyzer na ito ay may pinaka-primitive na disenyo (larawan sa itaas). Ang mga ito ay nailalarawan sa pamamagitan ng katangian na ang pagmamanipula sa bilang ng mga cell ay magbibigay sa iyo ng pagkakataon na paandarin ang aparato mula sa isang mapagkukunan na may anumang boltahe.
Dumadaloy na view
Ang mga yunit na ito ay may sa kanilang sariling disenyo ng isang bathtub na ganap na puno ng electrolyte na may mga elemento ng electrode at isang reservoir.
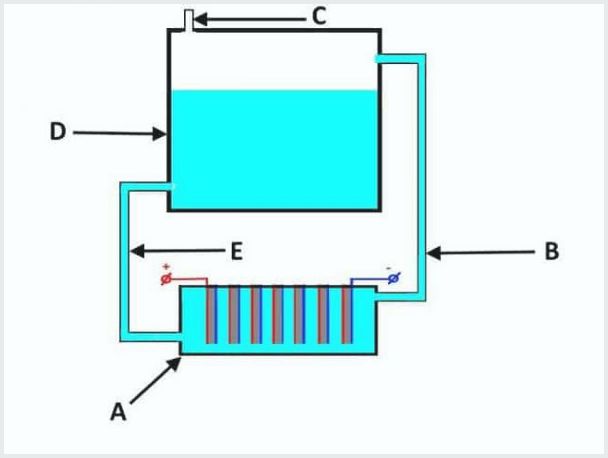

Ang aparato ng isang maginoo na daloy-sa pamamagitan ng electrolyzer, kung saan ang A ay isang paliguan na may mga electrode, ang D ay isang tangke, B, E ay mga tubo, ang C ay isang balbula ng outlet
Ang prinsipyo ng pagtatrabaho ng flow-through electrolysis plant ay ang mga sumusunod (mula sa larawan sa itaas):
- kapag ang paglabas ng electrolysis, ang electrolyte ay pinipiga nang sabay-sabay sa gas sa pamamagitan ng tubo na "B" papunta sa tangke na "D";
- sa tangke na "D" ang proseso ng paghihiwalay ng gas mula sa mga daloy ng electrolyte;
- paglabas ng gas sa pamamagitan ng balbula na "C";
- ang solusyon sa electrolyte ay dumadaloy pabalik sa pamamagitan ng tubong "E" upang maligo ang "A".
Nakatutuwang malaman. Ang prinsipyo ng pagtatrabaho na ito ay na-set up sa ilang mga inverter machine - ang pagkasunog ng pinakawalan na gas ay nagpapahintulot sa mga bahagi na ma-welding.
Tanawin ng lamad
Ang isang lamad na halaman ng electrolysis ay may parehong disenyo tulad ng iba pang mga electrolyser, ngunit ang electrolyte ay isang polymer-based solid na tinatawag na membrane tissue.
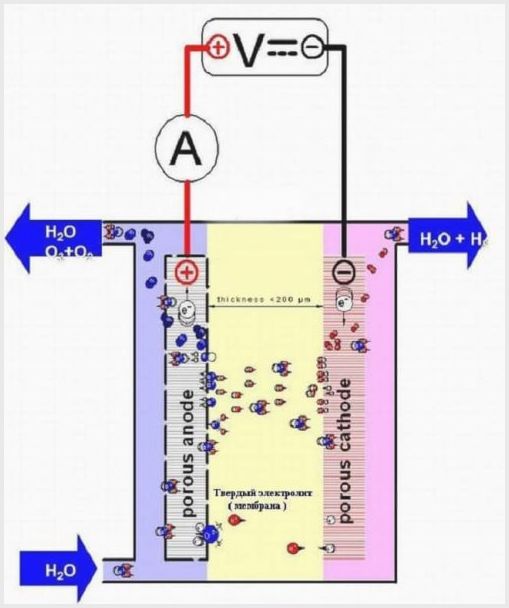

Disenyo ng membrane electrolyzer
Ang tisyu ng lamad sa naturang mga pinagsama-sama ay may dalawahang layunin - ang paglipat ng mga ions at proton, ang pag-zoning ng mga electrode at electrolysis na produkto.
Pagtingin ng diaphragm
Kapag ang isang sangkap ay hindi maaaring tumagos at makaapekto sa iba pa, isang porous diaphragm ang ginagamit, na maaaring gawin ng salamin, mga hibla ng polimer, ceramika o materyal na asbestos.
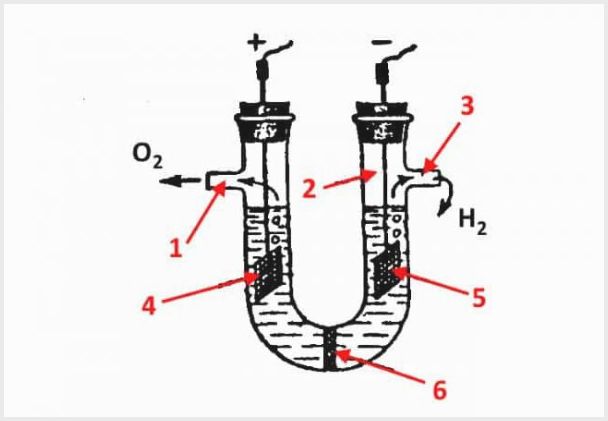

Ang aparato ng isang diaphragm electrolyzer, kung saan ang 1 ay isang outlet para sa oxygen, 2 ay isang flask, 3 ay isang outlet para sa hydrogen, 4 ay isang anode, 5 ay isang cathode, 6 ay isang dayapragm
Alkalina
Ang elektrolisis ay hindi maaaring maganap sa dalisay na tubig. Sa ganitong mga kaso, kinakailangan na gumamit ng mga catalista, na mga solusyon sa alkalina na may mataas na konsentrasyon. Batay dito, ang isang makabuluhang bahagi ng mga ionic device ay maaaring tawaging alkalina.
Ang pangunahing bagay! Dapat pansinin na ang paggamit ng asin bilang isang katalista ay nakakapinsala, dahil ang chlorine gas ay inilabas habang ginagawa ang reaksyon. Bilang panuntunan, ang sodium hydroxide ay kumikilos bilang isang kamangha-manghang katalista, na hindi pumipasok sa mga metal electrode at hindi nag-aambag sa pagpapalabas ng mga nakakapinsalang sangkap.
Gumawa ng sariling electrolyzer
Ang sinuman ay maaaring gumawa ng isang electrolyzer gamit ang kanilang sariling mga kamay. Para sa proseso ng pagpupulong ng pinaka-karaniwang disenyo, kakailanganin ang mga sumusunod na materyales:
- hindi kinakalawang na asero sheet (ang pinakamahusay na mga pagpipilian ay mga banyagang AISI 316L o atin 03X16H15M3);
- bolts М6х150;
- mga hugasan at mani;
- transparent tube - maaari kang gumamit ng antas ng espiritu, na ginagamit para sa mga hangarin sa pagtatayo;
- maraming mga herringbone fittings na may isang panlabas na diameter ng 8 mm;
- lalagyan ng plastik na may dami na 1.5 liters;
- isang maliit na pansala ng pag-filter ng tubig sa gripo, halimbawa, isang filter para sa mga washing machine;
- di-bumalik na balbula ng tubig.
Proseso ng Assembly
Kolektahin ang electrolyzer gamit ang iyong sariling mga kamay alinsunod sa mga sumusunod na tagubilin:
- Una sa lahat, kailangan mong markahan at ang kasunod na paglalagari ng sheet na hindi kinakalawang na asero sa magkaparehong mga parisukat. Ang paglalagari ay maaaring gawin sa isang gilingan ng anggulo (anggiling gilingan). Ang isa sa mga sulok sa gayong mga parisukat ay dapat i-cut sa isang anggulo upang ma-secure ang mga plate nang tama;
- Susunod, kailangan mong gumawa ng isang butas para sa bolt sa gilid ng plato sa tapat mula sa sulok ng lagari na gupitin;
- Ang koneksyon ng mga plato ay dapat gawin sa pagliko: isang plato sa "+", ang susunod sa "-" at iba pa;
- Sa pagitan ng magkakaibang singil na mga plato dapat mayroong isang insulator, na gumaganap bilang isang tubo mula sa antas ng espiritu. Dapat itong i-cut sa mga singsing, na dapat i-cut pahaba upang makakuha ng mga piraso ng 1 mm kapal. Ang distansya sa pagitan ng mga plato ay sapat para sa mahusay na evolution ng gas sa panahon ng electrolysis;
- Ang mga plato ay nakakabit nang magkasama gamit ang mga washer tulad ng sumusunod: ang isang washer ay nakaupo sa bolt, pagkatapos ay isang plato, pagkatapos ay tatlong mga washer, pagkatapos ng isang plato, at iba pa. Ang mga plato, pinapaboran na sisingilin, ay inilalagay sa isang mirror na imahe ng mga negatibong sisingilin na sheet. Ginagawang posible upang mapigilan ang mga gilid na gabas na hawakan ang mga electrode;


Ang mga plate ng planta ng electrolysis ay nagtipon-tipon
- Kapag pinagsama ang mga plato, dapat mong sabay na ihiwalay ang mga ito at higpitan ang mga mani;
- Gayundin, ang bawat plato ay dapat na ring upang matiyak na walang maikling circuit;
- Dagdag dito, ang buong pagpupulong ay dapat ilagay sa isang plastik na kahon;
- Pagkatapos nito, sulit na i-highlight ang mga lugar kung saan hinahawakan ng mga bolt ang mga dingding ng lalagyan, kung saan ka drill ng dalawang butas. Kung ang mga bolt ay hindi umaangkop sa lalagyan, pagkatapos ay kailangan nilang i-cut sa isang hacksaw;
- Pagkatapos ang mga bolt ay hinihigpit ng mga mani at washers para sa higpit ng istraktura;


Mga plato na inilagay sa isang lalagyan ng plastik
- Matapos ang mga hakbang na ginawa, kakailanganin mong gumawa ng mga butas sa takip ng lalagyan at ipasok ang mga fittings sa kanila. Ang impermeability sa kasong ito ay maaaring matiyak sa pamamagitan ng pag-sealing ng mga kasukasuan na may mga silanteng nakabatay sa silicone;
- Ang isang balbula ng kaligtasan at filter sa istraktura ay matatagpuan sa gas outlet at nagsisilbing isang paraan ng pagkontrol sa labis na akumulasyon ng gas, na maaaring humantong sa hindi magandang resulta;
- Ang yunit ng electrolysis ay binuo.
Ang huling yugto ay isang pagsubok, na ginaganap sa katulad na paraan:
- pagpuno ng lalagyan ng tubig hanggang sa marka ng mga bolts para sa mga fastener;
- pagkonekta ng lakas sa aparato;
- koneksyon sa pag-angkop ng tubo, ang kabaligtaran na dulo nito ay ibinaba sa tubig.
Kung ang isang mahina na kasalukuyang ay inilalapat sa pag-install, pagkatapos ang paglabas ng gas sa pamamagitan ng tubo ay halos hindi mahahalata, ngunit posible na panoorin ito mula sa loob ng electrolyzer. Sa pamamagitan ng pagdaragdag ng kasalukuyang alternating, pagdaragdag ng isang alkaline catalyst sa tubig, posible na makabuluhang taasan ang ani ng puno ng gas na sangkap.
Ang ginawang electrolyzer, bilang panuntunan, ay isang mahalagang bahagi ng maraming mga aparato, halimbawa, isang hydrogen burner.


ang hitsura ng isang hydrogen burner, ang batayan nito ay itinuturing na isang self-made electrolyzer
Alam ang mga uri, pangunahing katangian, aparato at prinsipyo ng pagtatrabaho ng mga ionic na pag-install, maaari mong maisagawa ang tamang pagpupulong ng isang istrakturang ginawa ng bahay, na kung saan ay isang mahusay na katulong sa iba't ibang mga pang-araw-araw na sitwasyon: mula sa hinang at pag-save ng pagkonsumo ng gasolina ng mga sasakyan sa motor ang paggana ng mga sistema ng pag-init.
Gawin ang electrolyser gamit ang iyong sariling mga kamay
Tiyak, pamilyar ka sa proseso ng electrolysis mula sa kurikulum sa elementarya. Ito ay kapag ang 2 polar electrodes ay inilalagay sa tubig sa ilalim ng kasalukuyang upang makakuha ng mga metal o di-metal sa kanilang dalisay na anyo. Kailangan ng electrolyzer upang mabulok ang mga molekula ng tubig sa oxygen at hydrogen. Ang electrolyser, bilang bahagi ng mga mekanismong pang-agham, ay hinahati ang mga molekula sa mga ions.
Mayroong dalawang uri ng aparatong ito:
- Dry electrolyzer (ito ay isang ganap na sarado na cell);
- Basang electrolyzer (ito ang dalawang metal plate na nakalagay sa isang lalagyan ng tubig).
Ang aparato na ito ay simple sa mga tuntunin ng aparato, na ginagawang posible gamitin kahit sa bahay... Hinahati ng mga electrolyzer ang mga singil ng electrolysis ng mga atomo ng mga molekula sa mga singil na atomo.
Sa aming kaso, hinahati nito ang tubig sa positibong hydrogen at negatibong oxygen. Upang magawa ito, isang malaking halaga ng enerhiya ang kinakailangan, at upang mas mababa ang kinakailangang dami ng enerhiya, ginamit ang isang katalista.
Produksyon ng hydrogen sa pamamagitan ng electrolysis ng tubig
Ang pagkuha ng purong hydrogen sa pamamagitan ng electrolysis ng tubig ay ang pinaka halata at mabisang teknolohiya, at isa sa pinaka promising paraan upang makakuha ng mga alternatibong fuel. Ang hydrogen ay nakuha mula sa anumang may tubig na solusyon, at kapag sinunog, ito ay bumalik sa tubig.
Kung ihahambing sa iba pang mga pamamaraan ng paggawa ng hydrogen, ang electrolysis ng tubig ay may bilang ng mga kalamangan. Una, ginagamit ang magagamit na mga hilaw na materyales - demineralized na tubig at elektrisidad. Pangalawa, walang mga nagpapalabas ng polusyon sa panahon ng paggawa. Pangatlo, ang proseso ay ganap na awtomatiko. Sa wakas, ang output ay isang medyo puro (99.99%) na produkto. Sa lahat ng mga pamamaraan ng electrolysis, ang electrolysis na may mataas na temperatura ay itinuturing na pinaka-maaasahan (ang halaga ng hydrogen ay mula sa $ 2.35 hanggang $ 4.8 / kg). Dapat itong armadong teknolohikal, dahil sa ilalim ng ilang mga kundisyong pang-ekonomiya maaari itong magamit sa isang malakihang antas ng industriya.
Ang electrolysis ng tubig ay isang proseso ng physicochemical kung saan ang dalisay na tubig ay nabubulok sa oxygen at hydrogen sa ilalim ng impluwensya ng isang pare-pareho na kasalukuyang kuryente. Bilang isang resulta ng paghihiwalay ng mga molekula ng tubig sa mga bahagi, ang hydrogen ay nakuha sa dami ng dalawang beses na mas maraming oxygen. Ang kahusayan ng electrolysis ay tulad ng tungkol sa isang metro kubiko ng parehong mga gas ay nakuha mula sa 500 ML ng tubig sa halagang tungkol sa 4 kW / h ng elektrikal na enerhiya.
Ang kasalukuyang proseso para sa proseso ng electrolysis ng tubig upang makakuha ng hydrogen at oxygen ay nakuha, bilang isang panuntunan, sa tulong ng isang pang-industriya na tagatama na may kinakailangang mga parameter ng pagpapatakbo, Karaniwan ang boltahe na ito ay hanggang sa 90V at kasalukuyang lakas hanggang sa 1500 A. Ang isang naaangkop na yunit ay Pulsar SMART.
Sa elektronikong pagpapakita ng rectifier Pulsar SMART o sa espesyal na software para sa isang computer, makokontrol mo ang lahat ng mga yugto ng proseso ng paggawa, na nagbibigay-daan sa operator na subaybayan ang mga parameter at i-log ang pag-usad ng teknolohikal na proseso sa buong oras. Ganap na awtomatikong pagpapatakbo kasama ang patuloy na pagsubaybay sa lahat ng mga parameter para sa walang kaguluhan na operasyon nang walang pangangasiwa ng operator. Ang lahat ng mga parameter na nauugnay sa boltahe at kasalukuyang ay patuloy na sinusukat at kinokontrol ng rectifier microprocessor. Bukod dito, ang lahat ng sinusubaybayan na mga parameter ay naayos ng isang aparato, kung saan, sa kaganapan ng isang pagkabigo o paglihis, maaaring awtomatikong itigil ang proseso at signal ito sa pamamagitan ng isang ilaw na haligi.
Ang mga Rectifier ng serye ng Pulsar SMART ay idinisenyo alinsunod sa pinakamataas na kinakailangan sa kahusayan sa industriya at pamantayan sa internasyonal. Sa parehong oras, pinapayagan ng teknolohikal na software ang kakayahang umangkop sa pagbagay sa mga kinakailangan ng Customer, at patuloy na pinapabuti.
Lumilikha kami ng isang aparato gamit ang aming sariling mga kamay
Ang aparato para sa prosesong ito ay maaaring gawin sa pamamagitan ng kamay.
Para dito kakailanganin mo:
- Hindi kinakalawang na asero sheet;
- Bolts M6 x 150;
- Mga washer;
- Mga mani;
- Transparent tube;
- Pagkonekta ng mga elemento na may thread sa magkabilang panig;
- Isa't kalahating litro na lalagyan ng plastik;
- Pansala ng tubig;
- Suriin ang balbula para sa tubig.
Ang isang mahusay na pagpipilian para sa hindi kinakalawang na asero ay ang AISI 316L mula sa isang banyagang tagagawa o 03X16H15M3 mula sa isang tagagawa mula sa ating bansa. Mayroong ganap na hindi na kailangang bumili ng hindi kinakalawang na asero, maaari mong kunin ang luma. 50 hanggang 50 sentimo ay sapat na para sa iyo.
"Bakit kumuha mismo ng hindi kinakalawang na asero?" - tinatanong mo. Dahil ang pinaka-karaniwang metal ay magwawalis. Mas tinitiis ng hindi kinakalawang na asero ang mga alkalis. Dapat balangkas ang sheet sa isang paraan upang hatiin ito sa 16 na magkatulad na mga parisukat... Maaari mo itong i-cut gamit ang isang gilingan ng anggulo. Sa bawat parisukat, gupitin ang isa sa mga sulok.
Sa kabilang panig at kabaligtaran na sulok, mula sa nawn-off na sulok, mag-drill ng isang butas para sa isang bolt na makakatulong na magkasama ang mga plato. Ang electrolyzer ay hindi titigil sa pagtatrabaho tulad nito:t plate kuryente dumadaloy sa plato - at ang tubig ay nabubulok sa oxygen at hydrogen. Salamat dito, kailangan namin ng isang mahusay at negatibong plato.
Ang mga plato ay dapat na magkonekta nang halili: plus-minus-plus-minus, na may katulad na pamamaraan, magkakaroon ng isang malakas na kasalukuyang. Upang ihiwalay ang mga plate isa mula sa isa, isang tubo ang ginagamit. Ang isang singsing ay pinutol mula sa antas. Sa pamamagitan ng pagputol nito, nakakakuha tayo ng isang strip millimeter na makapal. Ang distansya na ito ay mas tama para sa paggawa ng gas.
Ang mga plato ay magkakaugnay sa mga washer: inilalagay namin ang isang washer sa bolt, pagkatapos ay isang plato at tatlong mga washer, pagkatapos ay isang plato muli, at iba pa. Sa plus at minus, walong plato ang dapat itanim. Kung ang lahat ay tapos na nang tama, kung gayon ang mga pagbawas ng mga plato ay hindi hawakan ang mga electrode.
Pagkatapos ay kailangan mong higpitan ang mga mani at ihiwalay ang mga plato. Pagkatapos ay inilalagay namin ang istraktura sa isang lalagyan ng plastik.
Pag-debug at pagsubok ng aparato
Pagkatapos ito ay kinakailangan upang matukoy kung saan ang mga bolts ay hawakan ang mga dingding ng kahon at, sa mga lugar na iyon, mag-drill ng dalawang butas. Kung sa walang maliwanag na dahilan lumalabas na ang mga bolt ay hindi umaangkop sa lalagyan, kung gayon dapat gupitin at higpitan para sa higpit ng mga mani... Ngayon ay kailangan mong i-drill ang takip at ipasok ang mga sinulid na konektor doon mula sa magkabilang panig. Upang matiyak ang kawalang-tatag, ang magkasanib ay dapat na selyohan ng isang silicone-based sealant.
Matapos tipunin ang iyong sariling electrolyzer gamit ang iyong sariling mga kamay, dapat mo itong subukan. Upang magawa ito, ikonekta ang aparato sa isang mapagkukunan ng kuryente, punan ito ng tubig sa mga bolt, ilagay sa takip sa pamamagitan ng pagkonekta ng isang tubo sa angkop at pagbaba ng kabaligtaran na dulo ng tubo sa tubig. Kung mahina ang kasalukuyang, makikita ang kasalukuyang mula sa loob ng electrolyzer.
Unti-unting taasan ang kasalukuyang sa iyong homemade appliance. Ang distiladong tubig ay hindi mahusay na nagsasagawa ng kuryente sapagkat wala itong mga asing-gamot o impurities. Upang maihanda ang electrolyte, kinakailangan upang magdagdag ng alkali sa tubig. Upang magawa ito, kailangan mong kumuha ng sodium hydroxide (nakapaloob sa mga paraan para sa paglilinis ng mga tubo tulad ng "Mole"). Kailangan ng isang balbula sa kaligtasan upang maiwasan ang pag-iipon ng disenteng halaga ng gas.
- Mas mahusay na gamitin ang dalisay na tubig at soda bilang isang katalista.
- Dapat mong ihalo ang ilan sa baking soda na may apatnapung bahagi ng tubig. Ang mga pader sa gilid ay pinakamahusay na gawa sa acrylic na baso.
- Ang mga electrode ay pinakamahusay na gawa sa hindi kinakalawang na asero. Makatuwirang gumamit ng ginto para sa mga plato.
- Gumamit ng translucent PVC para sa pag-back. Maaari silang maging 200 by 160 millimeter sa laki.
- Maaari mong gamitin ang iyong sariling electrolyzer, na ginawa ng iyong sarili, upang magluto ng pagkain, para sa kumpletong pagkasunog ng gasolina sa mga kotse at sa karamihan ng mga kaso.
Pangunahing ginagamit ang mga dry electrolyzer para sa mga makina. Pinapataas ng generator ang lakas ng engine ng pagkasunog. Ang hydrogen ay nag-apoy nang mas mabilis kaysa sa likidong gasolina, na nagdaragdag ng lakas ng piston. Bilang karagdagan sa Mole, maaari kang kumuha ng Mister Muscle, caustic soda, baking soda.
Ang generator ay hindi gumagana sa inuming tubig.Mas mahusay na ikonekta ang kuryente tulad nito: ang una at ang huling plato - minus, at sa plato sa gitna - plus. Kung mas malaki ang lugar ng mga plato at mas malakas ang kasalukuyang, mas maraming gas ang pinakawalan.
DIY electrolysis sa bahay
Noong maliit pa ako, palagi kong nais na gumawa ng isang bagay sa aking sarili, gamit ang aking sariling mga kamay. Gayunpaman, karaniwang hindi pinapayagan ng mga magulang (at iba pang mga kamag-anak) na ito. At hindi ko nakita noon (at hindi pa rin nakikita) ang anumang mali kapag nais malaman ng maliliit na bata